- Improvement of Graphene Quality by Electrochemical Exfoliation using Polarity Reversing Potential
Sungmook Lim*, Wonoh Lee*†
* School of Mechanical Engineering, Chonnam National University
- 극성 변환 전압을 이용한 전기화학 박리 그래핀의 품질 개선
임성묵* · 이원오*†
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
In this study, we present a straightforward yet effective enhancement to the electrochemical exfoliation process, addressing graphene quality degradation caused by prolonged voltage application while ensuring a high yield. To minimize oxidation and defect formation resulting from interactions with active radicals and electrolyte ions during exfoliation, we implemented polarity-reversing potential technique with alternating voltage. This approach effectively removed oxygen functional groups from the exfoliated graphite surface while enabling efficient ion intercalation between graphite layers. As a result of this improved process, graphene with low defect density (ID/IG = 0.29) and high purity (C/O = 12.72) was successfully produced. Additionally, the graphene exhibited a 63% larger lateral size and 26% reduced thickness compared to conventional methods, highlighting its superior structural properties. Electrochemical performance evaluations further demonstrated a specific capacitance of 103.5 F g–1, —representing a 40% improvement — confirming significant enhancements in electrochemical performance.
고품질 그래핀의 대량생산은 그래핀의 다양한 응용 분야에서 산업적 활용을 실현하기 위한 핵심 과제로, 이를 목표로 여러 시도가 이루어지고 있다. 본 연구에서는 전기화학 박리 공정에서 전압 인가로 인한 그래핀 품질 저하문제를 해결하면서 높은 수율을 동시에 향상시킬 수 있는 간단한 개선 방안을 제안한다. 전기화학 박리 과정에서 활성 라디칼 및 전해질 이온과의 반응으로 발생하는 그래핀의 산화와 결함 형성을 억제하기 위해, 전압의 극성과 세기를 교대로 변환하는 기술을 도입하고 최적화하였다. 이를 통해 박리된 흑연 표면에 형성된 산소 작용기를 효과적으로 제거함과 동시에 흑연 층간의 이온 삽입 효율을 높였다. 이러한 공정 개선으로 결함 밀도가 낮은 (ID/IG = 0.29) 고순도 (C/O = 12.72) 그래핀을 생산할 수 있었다. 또한, 기존 공정에 비해 63% 더 큰 크기와 26% 더 얇은 두께를 나타내어 그래핀의 구조적 우수성을 확인하였다. 전기화학적 특성 평가 결과, 비정전용량이 103.5 F g–1로 40% 향상되었으며, 이를 통해 전기화학적 성능의 큰 개선을 입증하였다.
Keywords: 그래핀(Graphene), 전기화학 박리(Electrochemical exfoliation), 전기화학 특성(Electrochemical property), 극성 변환 전위(Polarity-reversing potential)
그래핀은 탄소 원자들이 sp2 혼성화를 통해 결합되어 배열된 2차원 나노 물질으로, 물리적·화학적·기계적 특성이 뛰어난 소재이다[1-3]. 뛰어난 전기전도성과 열전도성, 높은 기계적 강도, 넓은 비표면적 및 전자이동도 등의 물성은 그래핀을 다양한 응용 분야, 특히 에너지 저장 장치, 전자 소자, 센서 및 촉매 등에서 광범위하게 적용 가능한 물질로 주목받게 했다[4-6].
그래핀의 이러한 물성에 대한 응용 가능성을 실질적으로 구현하고 산업화하기 위해서는 고품질 그래핀을 대량으로 생산할 수 있는 기술이 필수적으로 요구된다. 현재 그래핀 생산을 위한 주요 방법으로는 기계적 박리법[7], 화학기상증착법(Chemical vapor deposition, CVD)[8], 산화 그래핀 환원법[9], 전기화학 박리법[10,11]이 있다.
기계적 박리법은 스카치테이프를 이용해 흑연에서 그래핀을 박리하는 방식으로, 높은 품질의 단층 그래핀을 생산할 수 있지만, 공정이 수작업에 의존하기 때문에 수율이 낮고 대량 생산이 불가능한 방식이다[12]. CVD는 구리 또는 니켈과 같은 금속 촉매 기판 위에서 메탄과 같은 탄화수소 기체를 1000–1200oC의 고온으로 분해하여 그래핀을 합성하는 방식이다. 이 방법은 고순도의 그래핀을 제조할 수 있지만, 고온 공정과 복잡한 장비가 필요하며 높은 비용으로 인해 산업적 활용에 제약이 있다[13]. 산화 그래핀 환원법은 대량 생산이 가능하다는 장점이 있지만, 환원 과정에서 필연적으로 다수의 결함이 발생하며 산소 작용기가 남게 되어 생성되는 그래핀의 품질이 낮다[14]. 또한, 대량의 화학 약품을 사용하기 때문에 투석 과정에서 많은 양의 정제수가 필요하며, 이로 인해 환경오염 문제가 발생할 수 있다.
전기화학 박리법은 흑연을 전극으로 사용하여 전해질에 담근 후 전압을 인가하여 전해질 이온을 흑연 층간에 삽입하고, 이온의 가스화를 통해 흑연 층간을 팽창시켜 반데르발스 결합을 해제하여 그래핀을 박리시키는 방식이다[15]. 이 방법은 고품질의 그래핀을 박리시킬 수 있으며, 공정이 단순하고 화학적 활성화를 통해 박리가 이루어지고 친환경적이기 때문에 그래핀의 대량 생산을 위한 유망한 방법으로 주목받고 있다. 특히 양전압을 이용한 음극 박리법은 양전압의 인가로 발생하는 수전해로 생성되는 HO·와 O·와 같은 활성 라디칼들이 흑연 층간 입구를 공격하여 팽창시키므로, 전해질 이온의 침투를 촉진시켜 높은 수율을 달성할 수 있으며, 얇고 큰 크기의 그래핀을 생산할 수 있다[10,16].
그러나 양전압을 장시간 인가하면 수전해로 생성된 다량의 활성 라디칼이 흑연을 지속적으로 공격하여 산화도가 증가하고, 박리된 그래핀의 결함이 많아지는 문제가 발생할 수 있다[17,18]. 이는 그래핀 품질 저하로 이어져 고품질 그래핀 생산을 방해하는 주요 문제점으로 작용하기 때문에 이러한 단점을 해결할 수 있는 간단하고 효율적인 접근 방식이 필요하다.
본 연구에서는 이러한 문제를 해결하기 위해 양전압과 음전압을 교대로 인가하는 극성 변환 전압 방법을 고안하였다. 양전압이 인가된 후 음전압을 적용하면, 흑연 표면에 형성된 산소 작용기와 라디칼을 효과적으로 제거할 수 있다. 또한, 극성 변화로 인해 흑연과 삽입 이온 간의 접촉 시간이 단축되어 그래핀의 산화를 방지할 수 있으며, 정전압 인가 방식에서 진동 효과를 적용한 것과 유사한 효과를 기대할 수 있다. 이를 통해 삽입 이온이 흑연층 내부로 더 깊숙이 침투할 가능성이 높아지고, 결과적으로 박리 효율을 개선하며 수율 증가와 더불어 박리된 그래핀의 형태적 개선도 이루어진다.
이 방법의 최적화를 위해 각 전압 인가 방식에 따른 박리 그래핀의 산화도, 결함도 및 수율 변화를 분석하였다. 분석 결과, 극성 변환 전압 방식은 전기화학적 박리 공정에서 그래핀의 산화와 결함 생성을 성공적으로 억제하면서도 박리 효율을 향상시킬 수 있음을 확인하였다. 또한, 박리된 그래핀의 전기화학적 특성을 분석하여 제안한 극성 변환 전기화학 박리법으로 생산된 그래핀의 품질과 신뢰성을 검토하였다.
2.1 재료
본 연구에서는 시그마 알드리치사의 플레이크 타입 흑연(325 mesh)을 사용하였다. 전기화학 박리 공정은 2전극 시스템에 기반하여, 작업 전극은 40 × 25 × 1 mm3 크기의 슬라이드 글래스에 전도성 카본 테이프를 부착한 후, 흑연 플레이크를 고정하여 제작하고, 상대 전극으로는 지름 2 mm의 원통형 백금 전극을 사용하였으며, 전해질은 0.1 M의 황산암모늄((NH4)2SO4)을 사용하였다.
2.2 전기화학 박리 실험
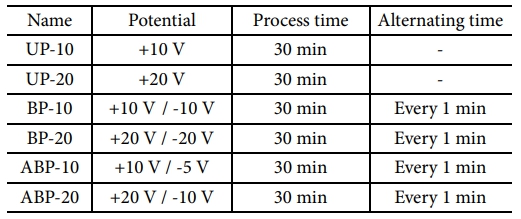
본 연구에서는 양극으로 흑연을 사용하고, 음이온을 삽입하는 2전극 음극 박리법을 기반으로 전기화학 박리가 진행되었다. 전기화학 박리 실험에서는 전해질에 담긴 전극의 크기와 전극 사이의 거리에 따른 영향을 배제하기 위해, 전극 전체를 전해질에 담그고 전극 사이의 거리는 1 cm로 고정하였다. 산성 전해질은 높은 전기화학 박리 효율을 보이지만 흑연의 산화에 따른 품질 저하가 발생하기 때문에[19], 이를 최소화하기 위해 수용성 무기 염 중 가장 낮은 환원 전위를 가져 우수한 박리 효율을 보이는 황산암모늄을 전해질로 사용하였다[15]. 전위의 인가는 파워 서플라이(Agilent, 33220A)를 사용하여, 기존의 방식인 단극성 전위(Unipolar potential, UP), 양극성 전위(Bipolar potential, BP) 및 비대칭 양극성 전위(Asymmetric bipolar potential, ABP)의 세 방법을 비교하였다. UP는 +10 V와 +20 V를 30분 동안, BP는 +10 V/-10 V와 +20 V/-20 V를 1분씩 번갈아가며 30분간, ABP는 +10 V/-5 V와 +20 V/-10 V를 1분씩 번갈아가며 30분 동안 인가하였다(Table 1).
2.3 특성 분석
박리된 그래핀의 형태 분석은 원자힘 현미경(Atomic force microscope, AFM)을 XE-100 (Park systems) 기기를 이용하여 수행하였다. 그래핀의 결함 분석은 레이저 라만 분광기(NRS-5100, JASCO, laser excitation: 532 nm)를 사용하여 진행되었으며, 박리 그래핀의 화학적 조성 분석은 Al-Kα (E = 1.487 keV) X선을 이용한 X선 광전자 분광법(X-ray photoelectron spectroscopy, XPS)을 XPS 분광기(K-ALPHA+, Thermo-fisher)를 사용하여 진행하였다. 또한, X선 회절 분석(X-ray diffraction, XRD)은 XRD 분석기(X'Pert PRO, PANalytical)를 통해 그래핀의 결정성을 분석하였다.
2.4 전기화학 특성 분석
박리된 그래핀의 전기화학적 특성을 조사하기 위해 유리탄소 전극의 표면에 그래핀을 코팅하여 작업 전극으로 사용하였다. 코팅된 그래핀의 양에 따른 전기화학 특성에 대한 영향을 최소화하고자, 모든 측정 샘플에 대해 동일한 양의 박리 그래핀을 코팅하였다. 상대 전극과 기준 전극으로는 각각 백금(Pt) 전극과 은/염화은(Ag/AgCl) 전극을 사용하였으며, 전해질로는 6.0 M 수산화 칼륨 용액을 사용하였다. 전기화학 실험은 전위가변기(PARSTAT 1000, Principal Applied Research) 장비를 이용하여 1 A g–1의 전류밀도에서 충·방전 시험(Galvanostatic charge-discharge, GCD)과 10, 50, 100 mV s–1의 스캔 속도에서 순환전압전류 시험(Cyclic voltammetry, CV)을 진행하였다. 각 GCD 및 CV 시험으로부터 비축전용량 CCD, CCV는 아래와 같이 계산하였다.

여기서 I는 전류밀도, m은 샘플의 질량, dV/dt는 GCD 시험에서 방전 곡선의 전위 기울기를 나타낸다. 또한 i와 V는 각각 전류와 전압이며, ∫idV는 CV 곡선의 적분 면적이다. 그리고 ΔV는 전압 범위, v는 스캔 속도이다.
3.1 그래핀의 화학적 특성과 수율 분석
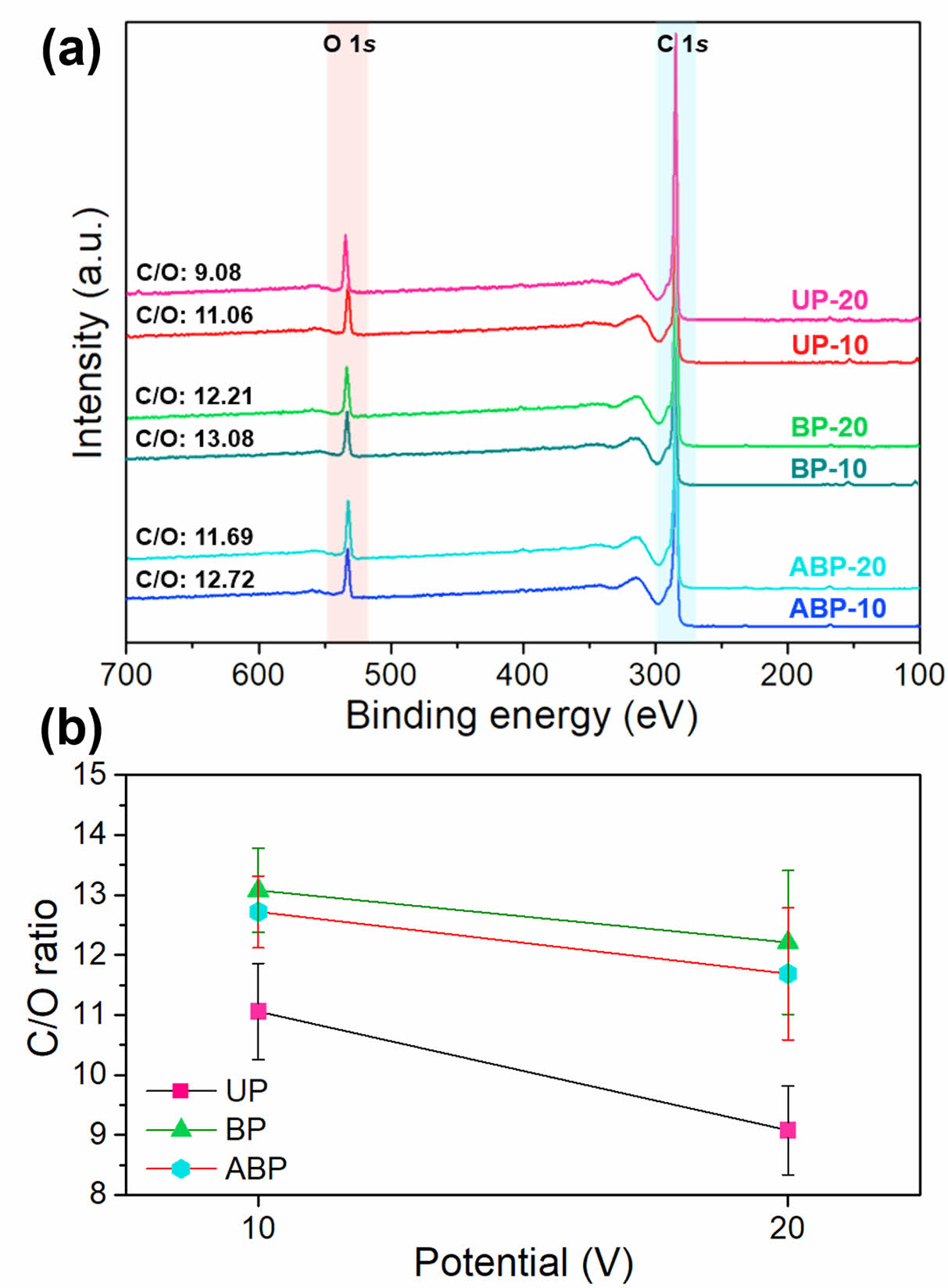
본 연구에서는 박리된 그래핀의 품질을 분석하기 위해 XPS 분석과 라만 분광 분석을 진행하였다. XPS 분석은 그래핀의 표면 원소 구성에 대한 중요한 정보를 제공한다. Fig. 1a에 나타낸 바와 같이, 모든 샘플에서 XPS 스펙트럼은 C 1s (284.5 eV)와 O 1s (532.3 eV)에서 뚜렷한 피크를 보였다. UP 그래핀(UP-10, UP-20)은 활성 라디칼의 지속적인 공격과 침투되는 산소 기반 삽입 이온과의 접
촉으로 인해 산화가 진행되어 낮은 C/O 비(UP-10: 11.06, UP-20: 9.08)을 나타냈다. 특히 UP-20의 경우, 더 높은 전압이 인가되면서 전해질 내에서 수전해가 더 많이 발생하여 더 높은 산화도를 보였다. 반면, BP 그래핀의 경우 양전압과 동일한 크기의 음전압을 인가함으로써 음전압 효과로 인해 박리된 그래핀의 산화를 성공적으로 억제할 수 있었기 때문에 높은 C/O 비를 보였다(BP-10: 13.08, BP-20: 12.21). ABP 그래핀은 상대적으로 낮은 크기의 음전압이 인가되었기 때문에 그래핀의 산화를 유발하는 이온 및 라디칼의 제거가 완벽히 이루어지지 않아 BP 그래핀보다는 낮은 C/O 비(ABP-10: 12.72, ABP-20: 11.69)를 보였으나, UP 그래핀보다는 높은 값을 나타냈다. 이러한 결과는 음전압 인가 효과로 인해 산소 작용기와 활성 라디칼이 박리 그래핀 표면에서 성공적으로 제거되었으며[20], 산소 작용기와의 접촉 시간이 절반으로 줄어들었기 때문에[21], 그래핀의 산화를 효과적으로 억제할 수 있었음을 보여준다(Fig. 1b).
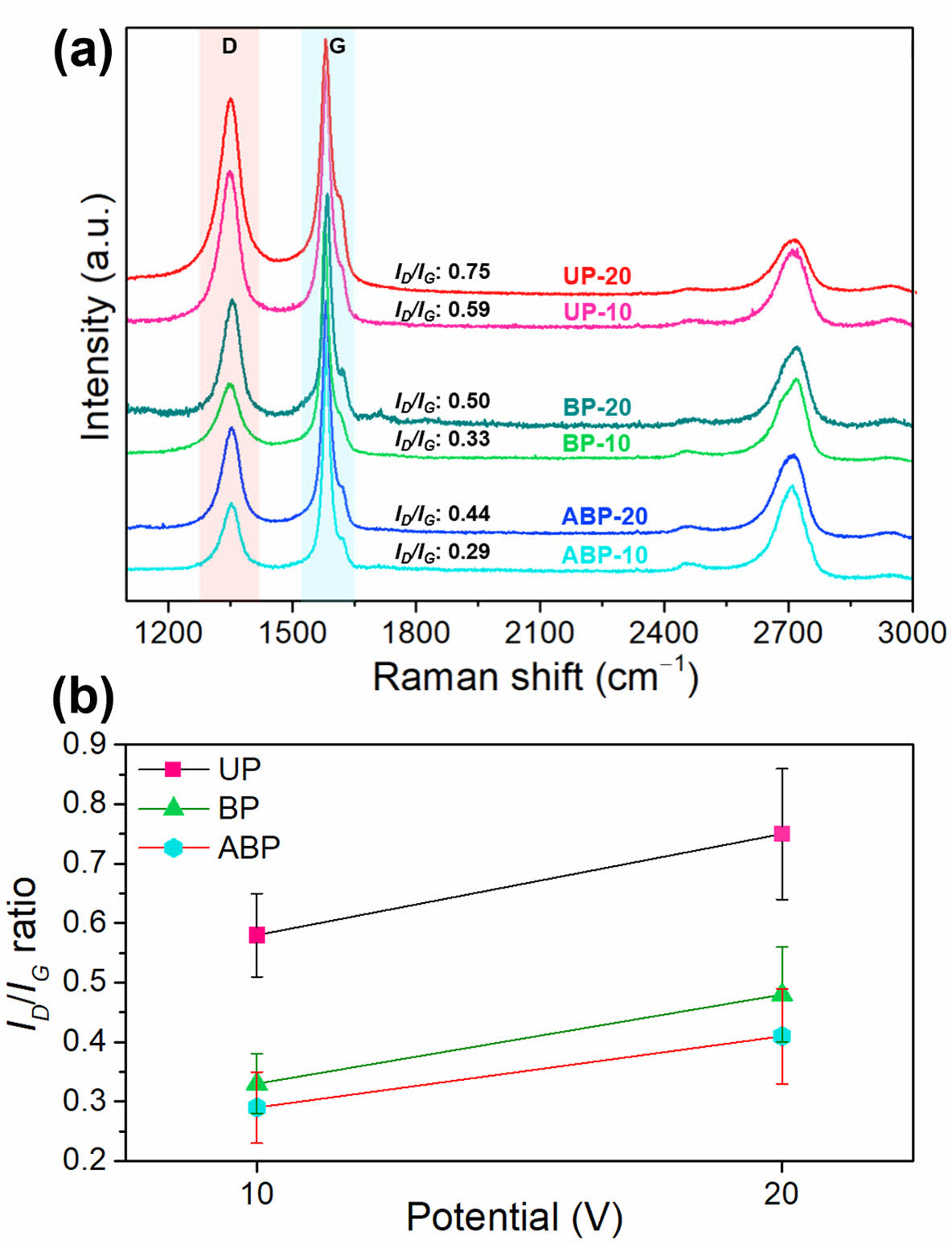
Fig. 2a에 나타된 그래핀 시트의 라만 스펙트럼은 그래핀에서 특징적으로 나타나는 D 밴드(~1350 cm–1)와 G 밴드 (~1580 cm−1)를 보여주었다. 여기서 D 밴드는 그래핀의 육각형 원자 구조에서 발생한 결함을 의미하며, G 밴드는 그래핀의 sp2 혼성화된 평면에서 탄소 원자의 진동을 의미한다[22]. D 밴드와 G 밴드의 강도 비율인 ID/IG는 그래핀의 원자 구조에서 결함의 정도를 나타내는 중요한 지표이다.
UP 그래핀의 경우, 활성 라디칼이 흑연 층간의 입구를 공격하여 팽창시키고 음이온이 침투함에 따라 그래핀에 결함이 필연적으로 발생한다. 이에 따라 UP-10과 UP-20은 각각 0.59와 0.75의 높은 ID/IG 값을 나타냈다. 반면, BP 및 ABP 그래핀은 음전압 인가를 통해 활성 라디칼을 지속적으로 제거함으로써 UP 그래핀에 비해 결함이 적었고, 낮은 ID/IG 값을 보였다. 주목할 점은 BP 그래핀(BP-10, BP-20)이 각각 0.33과 0.50의 ID/IG 값을 보이며 ABP 그래핀(ABP-10, ABP-20, 각각 0.29, 0.44)보다 더 높은 값을 기록했다는 점이다. 이는 높은 음전압이 인가된 경우, 양전압 인가를 통해 흑연 층간에 침투했던 음이온들이 빠져나오는 과정에서 상대적으로 빠른 속도로 흑연 층과 접촉하여 결함이 발생했기 때문으로 해석된다. 이러한 결과를 통해 BP 및 ABP 방식이 결함을 완전히 억제하지는 못했으나, Fig. 2b에서 확인할 수 있듯이 박리되는 그래핀의 결함 증가를 효과적으로 억제했음을 알 수 있다.
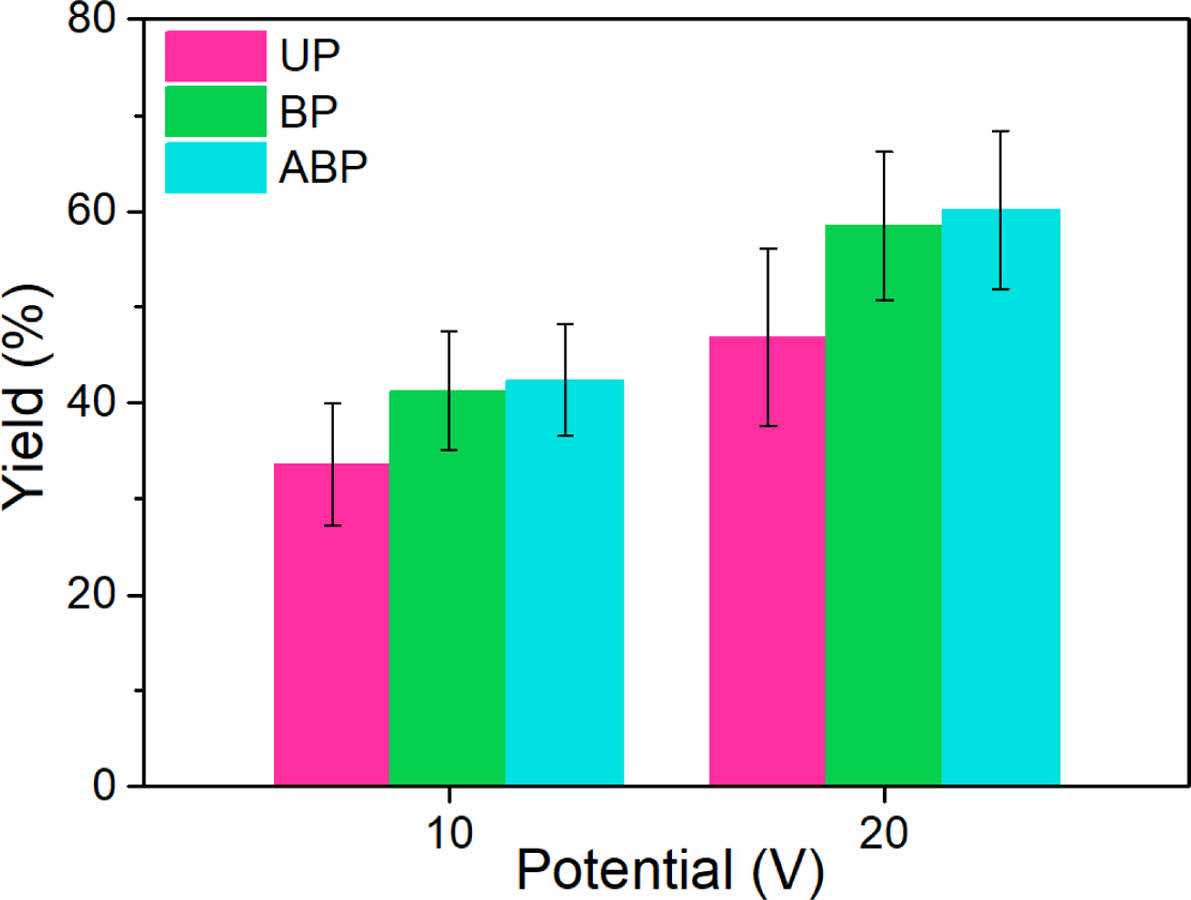
각 공정에 따른 전기화학 박리 공정의 수율은 Fig. 3에 도시하였다. UP-10과 UP-20은 삽입되는 SO42− 음이온(4.8 Å)과 흑연 층간거리(3.4 Å) 간의 차이로 인해 이온 침투 과정에서 병목 현상이 발생하였고[11], 이로 인해 낮은 수율을 보였다(UP-10: 33.64%, UP-20: 46.85%). 반면, BP와 ABP는 극성 변환 전압을 인가하여 이온 병목을 해소할 수 있었기 때문에 UP보다 높은 수율을 기록하였다. 특히 ABP (ABP-10: 42.38%, ABP-20: 60.15%)는 BP (BP-10: 41.28%, BP-20: 58.45%)보다 약간 더 높은 수율을 보였는데, 이는 약한 음전압이 인가된 상태에서 흑연 층간에 침투된 이온이 완전히 제거되지 않고 잔존함으로써 가스화를 통해 박리 반응이 추가적으로 진행된 결과로 해석된다. 이러한 박리 그래핀의 품질 개선과 수율 유지는 추가적인 공정, 첨가제, 또는 복잡한 이론 없이 달성되었다. 이는 전기화학 박리 공정에서 극성 변환법의 이점을 잘 보여주며, 장시간의 전압 인가를 통해 고수율과 동시에 고품질의 그래핀 박리가 가능함을 보여준다.
3.2 그래핀의 구조적 특성과 형태 분석
실험을 통해 얻은 그래핀의 품질과 수율을 바탕으로, 전기화학적 박리에서 그래핀의 품질과 수율 향상을 위한 극성 변환 전압의 최적 조건은 ABP-10으로 확인되었다. 본 연구에서는 박리된 그래핀의 형태 및 결정성 분석을 기존에 보고된 전기화학적 박리[15,16]에서 주로 사용되는 조건인 UP-10으로 박리된 그래핀과 비교하였다.
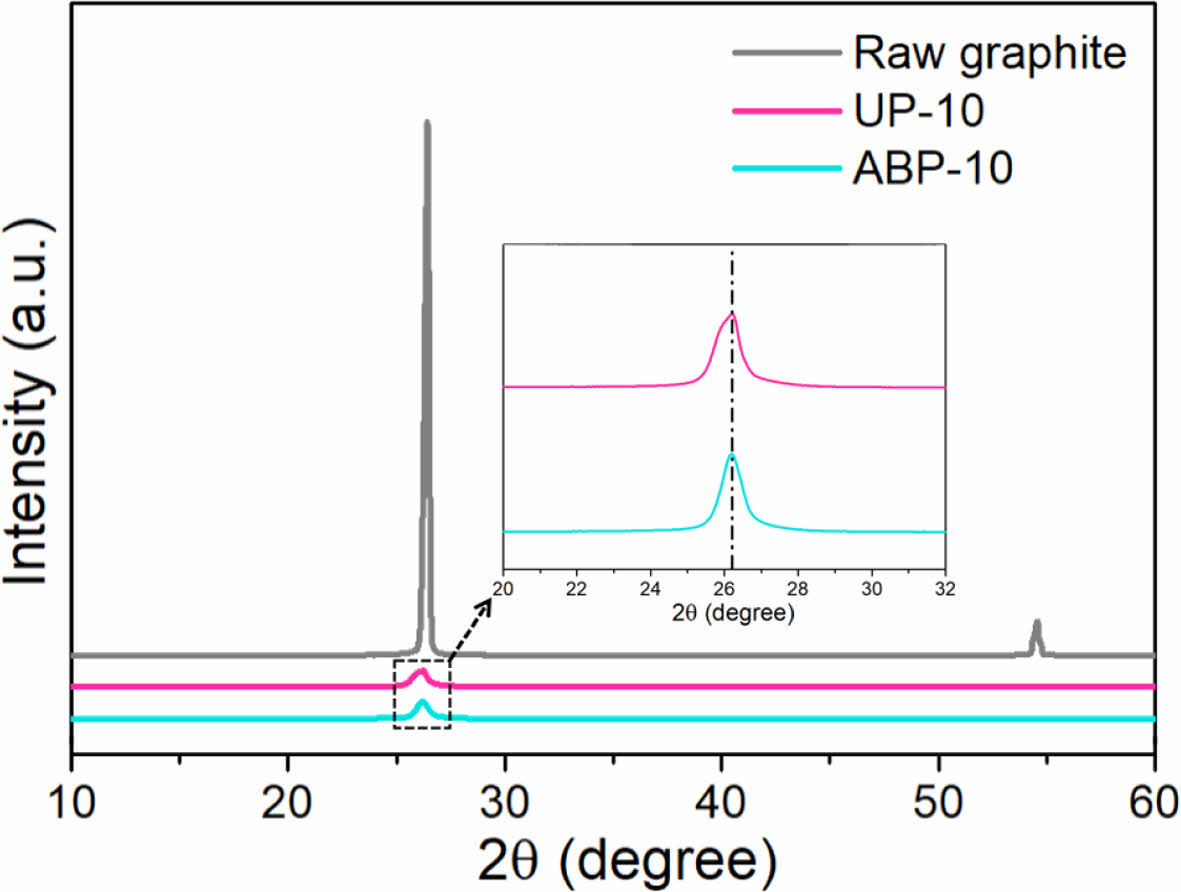
박리된 그래핀의 결정 구조를 조사하기 위해 XRD 분석을 수행하였다(Fig. 4). 흑연의 XRD 패턴은 약 26°에서 (002) 피크가 강하게 나타났다. 그래핀의 경우, 흑연에서 그래핀이 박리되면서 입자의 크기가 감소하여 회절 강도가 낮아졌다[23]. 그러나 Fig. 3에 삽입된 이미지에서 볼 수 있듯이, (002) 피크의 위치는 변하지 않았으며, 이는 UP-10 그래핀과 ABP-10 그래핀 모두 sp2 흑연 구조를 유지하고 있어 높은 결정성을 유지하고 있음을 확인할 수 있다.
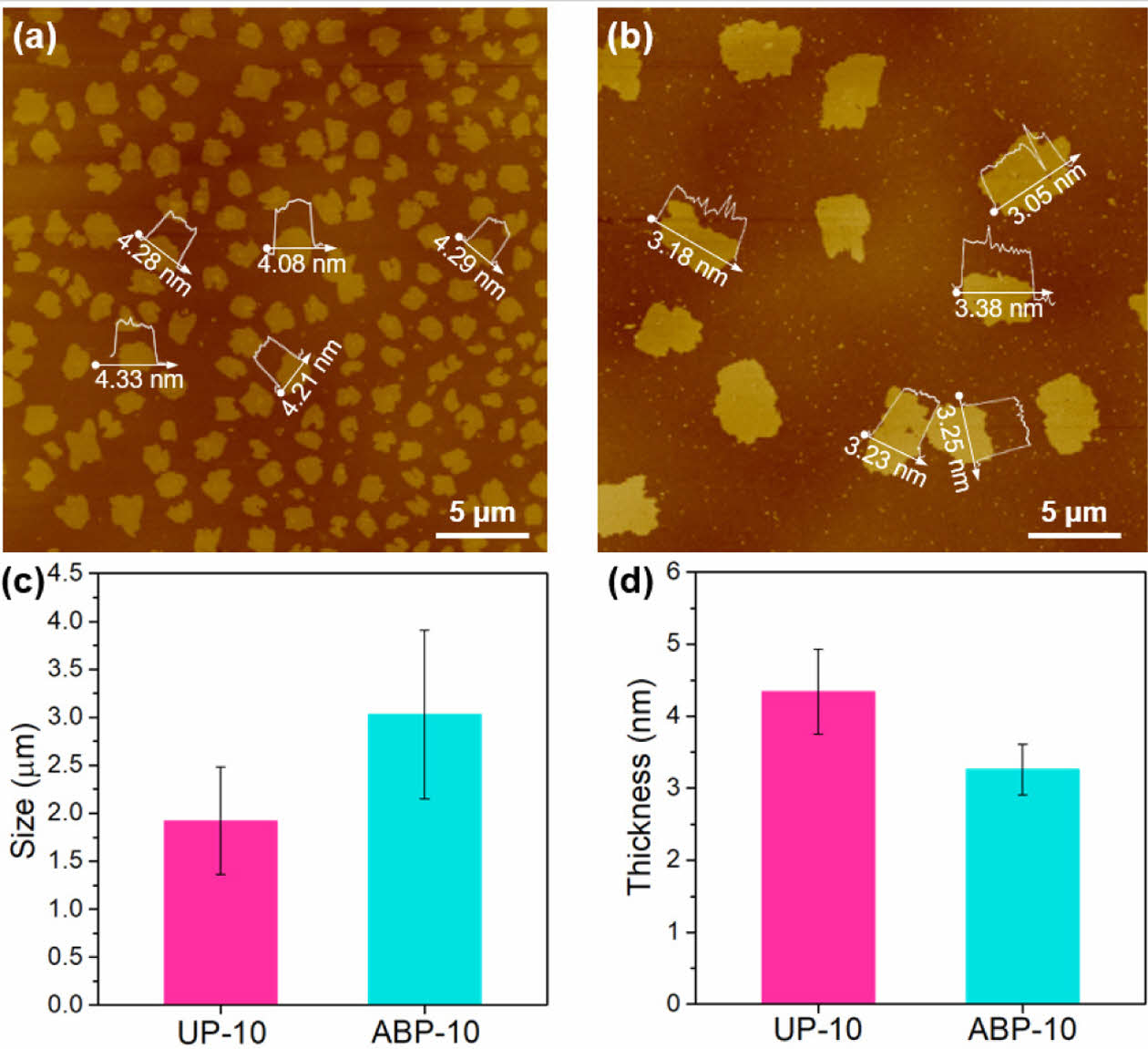
박리된 그래핀의 형태 분석을 위하여 AFM 분석을 수행하였으며, 그 결과는 Fig. 5a와 b에 제시되었다. 평균 크기는 스케일바로, 평균 두께는 그림 내에 별도의 프로파일로 명기하였다. UP-10 박리 그래핀은 평균 크기가 1.88 μm인 반면, ABP-10 박리 그래핀은 평균 크기가 3.07 μm로, 약 63% 더 큰 크기를 나타냈다(Fig. 5c), 평균 두께는 UP-10에서 4.38 nm로 측정된 반면, ABP-10은 3.26 nm로, 약 26% 더 얇은 그래핀이 박리되었음을 확인하였다(Fig. 5d). AFM 측정을 통해 실리콘 웨이퍼에 코팅된 단일 층 그래핀 시트의 두께(≒0.8 nm)를 기준으로 분석했을 때, 약 4층으로 이루어진 그래핀이 박리되었음을 알 수 있었다[24].
극성 변환 전압 박리법은 양전압과 음전압을 교대로 인가하는 방식으로, 전기화학 박리에서 발생할 수 있는 흑연 층간 입구에서의 전해질 이온 병목 현상을 해소할 수 있으며, 전압 극성의 지속적인 교대를 통해 이온을 흑연 층간으로 더욱 미세하고 깊숙이 침투시킴으로써 더 얇고 넓은 그래핀을 생산할 수 있었다. 본 연구 결과는 극성 변환 방식을 활용한 전기화학 박리법이 화학적, 구조적, 형태학적으로 우수한 그래핀을 생산할 수 있는 효과적인 방법임을 입증하며, 이는 그래핀의 전기적 및 전기화학적 특성 증대를 기대할 수 있음을 시사한다[25].
3.3 그래핀의 전기화학 특성 분석
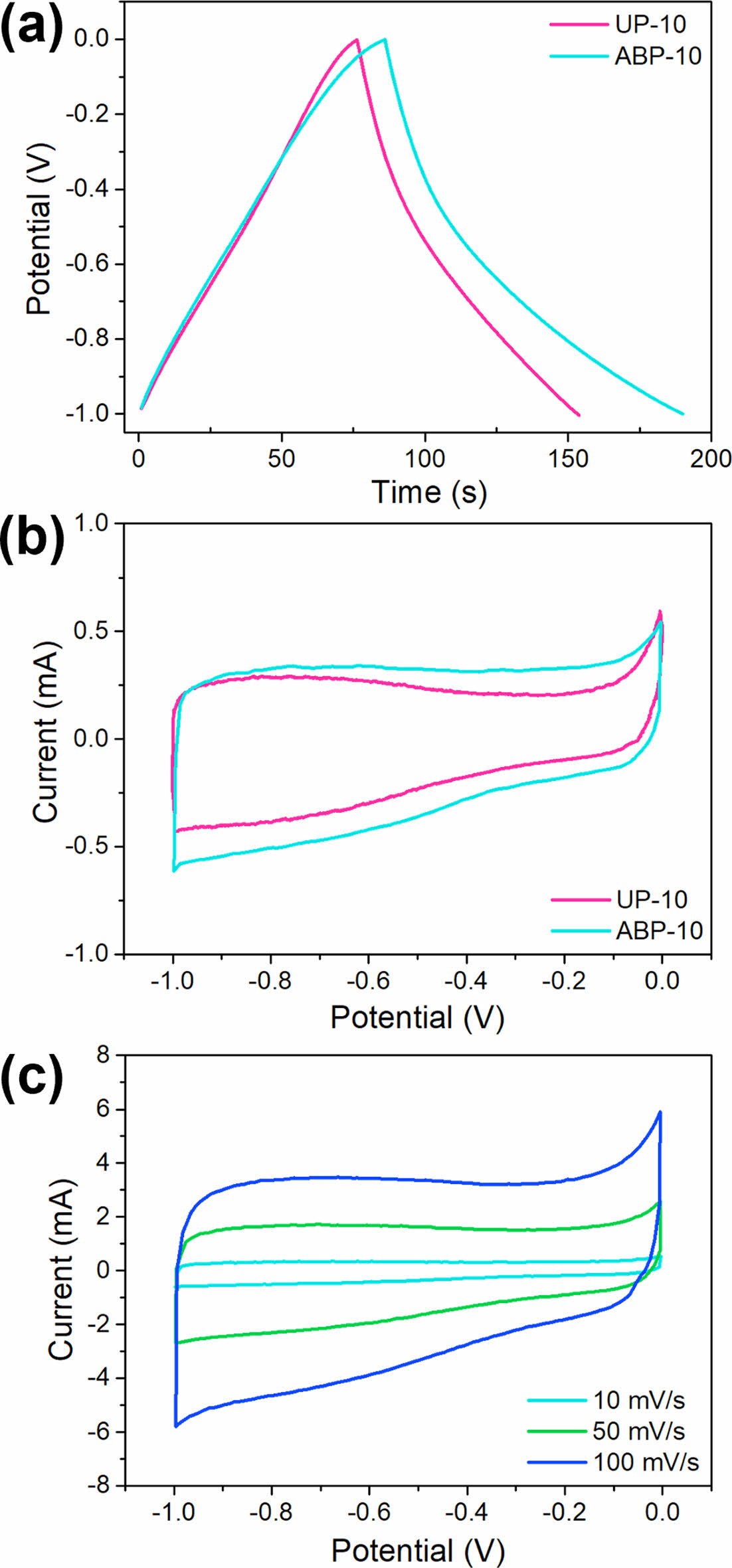
각 그래핀의 전기화학적 특성 분석 결과는 Fig. 6에 나타나있다. Fig. 6a에서 보여지는 삼각형 형상의 GCD 커브는 1.0 A g−1의 전류밀도에서 가역적인 용량성 거동을 나타낸다. ABP-10 그래핀은 UP-10에 비해 충전과 방전 시간이 더 길어, 더 나은 전류 응답을 제공하며, 더 많은 전해질 이온이 충방전 과정에 참여함으로써 높은 충방전 효율과 향상된 비정전용량을 보여준다. 이는 ABP-10 그래핀이 우수한 전기화학적 성능을 지님을 입증한다.
Fig. 6b는 -1.0~0.0 V의 전위 범위에서의 10 mV s−1의 스캔 속도로 측정된 CV 커브를 나타낸다. 두 그래핀 샘플 모두 준 직사각형 형상의 CV 곡선을 보여 전기이중층 정전용량 특성을 지닌다. 그러나 UP-10은 산소 작용기가 더 많이 포함되어 있어 산화환원 반응으로 인해 곡선의 형상이 직사각형을 유지하지 못하고 있다. 반면 ABP-10은 더 넓은 면적을 차지하며, 이는 ABP-10이 산소 작용기가 적은 고품질 그래핀임을 나타내며 더 높은 비정전용량을 지님을 증명한다. 이러한 결과는 ABP-10이 전하 저장 능력이 향상되어 고성능 에너지 저장 장치로의 응용 가능성을 가진 물질임을 시사한다.
Fig. 6c는 10~100 mV s−1의 스캔 속도로 측정한 ABP-10 그래핀의 CV 특성을 보여준다. CV 커브는 모든 스캔 속도에서 일관되게 준 직사각형 형상을 유지하였으며, 스캔 속도가 증가함에 따라 커브 면적과 전류 밀도가 비례하여 증가하였다. 이러한 결과는 높은 스캔 속도에서도 이온 확산과 전하 이동이 효율적으로 이루어지고 있음을 나타낸다.
이 결과, ABP-10의 비정전용량값은 CCD = 103.5 F g−1(CCV = 95.7 F g−1)으로 측정되어 UP-10의 CCD = 73.6 F g−1(CCV = 62.3 F g−1)보다 우수한 성능을 보였다. 이러한 개선은 산소 작용기 함량 및 결함도가 낮고, 더 넓고 얇은 그래핀을 박리할 수 있는 극성 변환 박리법의 효과를 입증한다. 이 방법은 빠른 이온 확산을 위한 최적화된 경로를 제공하며, 결과적으로 향상된 비정전용량을 가진 그래핀을 생산할 수 있는 혁신적인 방식임을 증명한다.
|
Fig. 1 (a) XPS survey scans results, and (b) the average C/O ratio of exfoliated graphene sheets |
|
Fig. 2 (a) Raman spectra results, and (b) the average ID/IG ratio of exfoliated graphene sheets |
|
Fig. 3 Yield percent of exfoliated graphene sheets |
|
Fig. 4 XRD patterns of exfoliated graphene sheets |
|
Fig. 5 AFM images of exfoliated graphene sheets: (a) UP-10, (b) ABP-10, and comparisons of (c) lateral size and (d) thickness |
|
Fig. 6 Electrochemical performance of the UP-10 and ABP-10 graphene sheets. (a) GCD curves at a current density of 1 A g−1, (b) CV curves at a scan rate of 10 mV s−1, and (c) CV curves of the ABP-10 graphene at different scan rates from 10 to 100 mV s−1 |
본 연구에서는 그래핀의 전기화학 박리법에서 장시간 전압 인가로 인해 발생하는 그래핀의 품질 저하 문제를 해결하기 위해 극성 변환 전압 방식을 제안하였다. 이 방법을 통해 박리된 그래핀은 전압이 인가되는 과정에서 산화 및 결함 생성을 성공적으로 억제하였고, 높은 수율을 보여주었다. 특히 생산된 ABP 그래핀은 기존 정전압 방식에 의한 UP 그래핀에 비해, 평균 크기가 63% 더 크고, 두께가 26% 더 얇으며 화학적, 구조적, 형태학적으로 우수한 특성을 지녔다. 이러한 ABP 방법에 의한 그래핀은 UP 그래핀 보다 40% 향상된 103.5 F g−1의 비정전용량을 나타내어 뛰어난 전기화학적 성능을 입증하였다. 본 연구는 장시간 전압 인가에서도 고품질과 높은 수율을 유지하면서 화학적, 형태적, 전기화학적 특성을 개선할 수 있는 간단하고 효율적인 접근법을 제시하였다. 이는 전기화학 박리법을 활용한 고품질 그래핀의 대량생산을 위한 실용적이고 효과적인 방법을 제안한다는 점에서 중요한 의의를 가진다.
본 연구는 과학기술정보통신부의 재원으로 한국연구재단과 교육부의 수소산업혁신인재양성사업의 지원을 받아 수행된 것이며, 이에 감사드린다(2021R1A2C2005751, 2022R1A6A3A13053740, 2024Hydrogen Industry-005).
- 1. Allen, M.J., Tung, V.C., and Kaner R.B., “Honeycomb Carbon: A Review of Graphene,” Chemical Reviews, Vol. 110, No. 1, 2009, pp. 132-145.
-

- 2. Huang, X., Yin, Z., Wu, S., Qi, X., He, Q., Zhang, Q., Yan, Q., Boey, F., and Zhang, H., “Graphene-Based Materials: Synthesis, Characterization, Properties, and Applications,” Small, Vol. 7, No. 14, 2011, pp. 1876-1902.
-

- 3. Yu, X., Cheng, H., Zhang, M., Zhao, Y., Qu, L., and Shi, G., “Graphene-based Smart Materials,” Nature Review Materials, Vol. 2, 2017, pp. 17046.
- 4. Xu, Y., Lin, Z., Zhong, X., Papandrea, B., Huang, Y., and Duan, X., “Solvated Graphene Frameworks as High-Performance Anodes for Lithium-Ion Batteries,” Angewandte Chemie International Edition, Vol. 54, No. 18, 2015, pp. 5345-5350.
-

- 5. Song, J., Yu, Z., Gordin, M.L., and Wang, D., “Advanced Sulfur Cathode Enabled by Highly Crumpled Nitrogen-Doped Graphene Sheets for High-Energy-Density Lithium-Sulfur Batteries,” Nano Letters, Vol. 16, No. 2, 2016, pp. 864-870.
-

- 6. Heerema, S.J., and Dekker, C., “Graphene Nanodevices for DNA Sequencing,” Nature Nanotechnology, Vol. 16, 2016, pp. 127-136.
- 7. Novoselov, K.S., Geim, A.K., Morozov, S.V., Jiang, D., Zhang, Y., and Dubonos, S.V., “Electric Field in Atomically Thin Carbon Films,” Science, Vol. 306, No. 5696, pp. 666-669.
-

- 8. Brownson, D.A.C., and Banks, C.E., “The Electrochemistry of CVDgraphene: Progress and Prospects,” Physical Chemistry Chemical Physics, Vol. 14, No. 23, 2012, pp. 8264-8281.
-

- 9. Hummers, W.S., and Offeman, R.E., “Preparation of Graphitic Oxide,” Journal of the American Chemical Society, Vol. 80, No. 6, 1958, pp. 1339.
-

- 10. Lu, J., Yang, J., Wang, J., Lim, A., Wang, S., and Loh, K.P., “One-pot Synthesis of Fluorescent Carbon Nanoribbons, Nanoparticles, and Graphene by the Exfoliation of Graphite in Ionic Liquids,” ACS Nano, Vol. 3, No. 8, 2009, pp.2367-2375.
-

- 11. Lim, S., Han, J.H., Kang, H.W., Lee, J.U., and Lee, W., “Preparation of Electrochemically Exfoliated Graphene Sheets Using DC Switching Voltages,” Carbon Letters, Vol. 30, 2020, pp.409-416.
- 12. Edwards, R.S., and Coleman, K.S., “Graphene Synthesis: Relationship to Applications,” Nanoscale, Vol. 5, No. 1, 2013, pp. 38-51.
-

- 13. Seekaew, Y., Phokharatkul, D., Wisitsoraat, A., and Wongchoosuk, Chatchawal, “Highly Sensitive and Selective Room-temperature NO2 Gas Sensor Based on Bilayer Transferred Chemical Vapor Deposited Graphene,” Applied Surface Science, Vol. 404, No. 15, 2017, pp. 357-363.
-

- 14. Eda, G., Fanchini, G., and Chhowalla, M., “Large-area Ultrathin Films of Reduced Graphene Oxide as a Transparent and Flexible Electronic Material,” Nature Nanotechnology, Vol. 3, 2008, pp. 270-274.
-

- 15. Parvez, K., Wu, Z., Li, R., Liu, X., Graf, R., Feng, X., and Müllen, K., “Exfoliation of Graphite into Graphene in Aqueous Solutions of Inorganic Salts,” Journal of the American Chemical Society, Vol. 136, No. 16, 2014, pp. 6083-6091.
-

- 16. Parvez, K., Li, R., Puniredd, S.R., Hernandez, Y., Hinkel, F., Wang, S., Feng, X., and Müllen, K., “Electrochemically Exfoliated Graphene as Solution-Processable, Highly Conductive Electrodes for Organic Electronics,” ACS Nano, Vol. 7, No. 4 2013, pp. 3598-3606.
-

- 17. Rao, K.S., Sentilnathan, J., Cho. H.W., Wu, J.J., and Yoshimura, M., “Soft Processing of Graphene Nanosheets by Glycine-Bisulfate Ionic-Complex-Assisted Electrochemical Exfoliation of Graphite for Reduction Catalysis,” Advanced Functuonal Materials, Vol. 25, No. 2, 2015, pp. 298-305.
-

- 18. Eredia, M., Bertolazzi, S., Leydecker, T., Garah, M.E., Janica. I., Melinte, G., Erson, O., Ciesielski, A., and Samori, P., “Morphology and Electronic Properties of Electrochemically Exfoliated Graphene,” The Journal of Physical Chemistry Letters, Vol. 8, No. 14, 2017, pp. 3347-3355.
-

- 19. Lee, H., Choi, J.I., Park, J., Jang, S.S., and Lee, S.W., “Role of Anions on Electrochemical Exfoliation of Graphite into Graphene in Aqueous Acids,” Carbon, Vol. 167, pp. 816-825.
-

- 20. Wang, X., Kholmanov, I., Chou, H., and Ruoff, R.S., “Simultaneous Electrochemical Reduction and Delamination of Graphene Oxide Films,” ACS Nano, Vol. 9, No. 9, 2015, pp. 8737-8743.
-

- 21. Liu, F., Wang, C., Sui, X., Riaz, M.A., Xu, M., Wei, L., and Chen, Y., “Synthesis of Graphene Materials by Electrochemical Exfoliation: Recent Progress and Future Potential,” Carbon Energy, Vol. 1, No. 2, 2019, pp. 173-199.
-

- 22. Wu, J., Lin, M., Cong, X., Liu, H., and Tan, P., “Raman Spectroscopy of Graphene-based Materials and Its Applications in Related Devices,” Chemical Society Reviews, Vol. 47, 2018, pp. 1822-1873.
-

- 23. Hu, L., Peng, X., Li, Y., Wang, L., Huo, K., Lee, L.Y.S., Wong, K.Y., and Chu, P.K., “Direct Anodic Exfoliation of Graphite onto High-density Aligned Graphene for Large Capacity Supercapacitors,” Nano Energy, Vol. 34, 2017, pp. 515-523.
-

- 24. Lotya, M., Hernandez, Y., King, P.J., Smith, R.J., Nicolosi, V., Karlsson, L.S., Blighe, F.M., De, S., Wang, Z., McGovern, I.T., Duesberg, G.S., and Coleman, J.N., “Liquid Phase Production of Graphene by Exfoliation of Graphite in Surfactant/Water Solutions,” Journal of the American Chemical Society, Vol. 131, No. 10, 2009, pp. 3611-3620.
-

- 25. Fang, X., Yu, X., Zheng, H., Jin, H., Wang, L., and Cao, M., “Temperature- and Thickness-dependent Electrical Conductivity of Few-layer Graphene and Graphene Nanosheets,” Physics Letters A, Vol. 379, No. 37, 2015, pp. 2245-2251.
-

 This Article
This Article
-
2024; 37(6): 499-505
Published on Dec 31, 2024
- 10.7234/composres.2024.37.6.499
- Received on Dec 15, 2024
- Revised on Dec 21, 2024
- Accepted on Dec 23, 2024
 Services
Services
Shared
 Correspondence to
Correspondence to
- Wonoh Lee
-
* School of Mechanical Engineering, Chonnam National University
- E-mail: wonohlee@jnu.ac.kr






 Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.
Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.