- Research of Thermal Properties for Liquid Crystalline Epoxy Composites with Tin Oxide Filler
Ha Nuel Hyun*, Seung Hyun Cho*†
* Department of Organic Materials and fiber Engineering, Soong-sil University
*† Department of Organic Materials and fiber Engineering, Soong-sil University- 산화주석을 함유한 열경화성 액정 에폭시의 열적 특성에 관한 연구
현하늘* · 조승현*†
A liquid crystalline thermosetting-epoxy-based
composite was fabricated using diglycidyl ether of 4,4'-biphenol, tin(IV) oxide
as a filler, and sulfanilamide as a curing agent. To investigate the thermal
behavior, Thermogravimetric Analysis and Laser Flash Apparatus were performed using
3.0−7.0 wt% Tin(IV) oxide. The
result showed that the activation energy and thermal conductivity were
proportional to the amount of added filler
Diglycidyl ether of 4,4'-biphenol을 기지로 사용하고,
tin(IV) oxide를 filler로,
sulfanilamide를 경화제로 사용하여 액정성 열경화성 에폭시 기반 복합재료를 제작하였다.
TGA와 LFA를 이용하여 3.0-7.0 wt%의 tin(IV) oxide를 분산시켜 제작한 복합재료의 열적 거동을 조사한 결과,
열분해 활성화 에너지와 열전도성이 filler의 첨가량에 비례하는 것으로 나타났다
Keywords: 열경화성 액정 에폭시(Liquid crystalline thermosetting epoxy), 산화주석(Tin oxide), 열분해 활성화 에너지 (Activation energy for thermal decomposition), 열전도도(Thermal conductivity)
현재 에폭시 수지는 기계적, 화학적, 전기적 특성이 우수하고 높은 구조 안정성을 가져 고체 절연 개폐기(solid insulated
switchgear, SIS)나 가스 절연 개폐기(gas insulated switchgear, GIS)의 절연 시스템같은
전기, 전자 계통에서 사용, 응용되고 있으며, 우주항공분야에서도 사용되고 있다[1-4]. 이러한 에폭시 수지는 전반적인 특성이 우수하지만 점도가
높고 경화시 열 수축이 일어난다는 단점이 존재하며, 주로 사용되는 전자, 전기 계통에서의 소형화 및 집적화로 인해 더 높은 열적 특성이 필요 해졌다[5].
때문에 이러한 단점을 보완하기 위해 액정성 에폭시가 주목을 받아왔다. 액정성 에폭시는 강직한 주쇄를 가져 특정 온도 구간에서 자체적으로 배향하는
특징을 가지며, 이를 이용해 말단의 에폭시기를 반응기로 하여 배향성을 제어할 수 있어 열수축을 방지할 수 있다[6]. 또한 액정성으로 인하여 기존의
범용 에폭시 대비 열전도도가 높다는 장점이 있으며[7], 특히 모노머에 큰 방향족 고리를 포함한 액정 고분자의 경우, 배향에 따른 이방성이 나타난다는
단점이 존재하지만, 높은 열저항성을 갖는다는 보고가 있다[8,9]. 본 실험에서는 메소젠으로 biphenyl기를 갖는 Diglycidyl
ether of 4,4-bisphenol (DGEBP)를 사용하였다. DGEBP의 경우 강직한 방향족
고리를 주쇄에 포함해 열 저항성이 커 전자, 전기분야에서 사용 시 범용 에폭시 대비 변형이 적을 것으로 생각된다. 또한 경화제로는
Sulfanilamide(SAA)를 사용하였는데, SU 등의 연구에 따르면 BP와 SAA를 사용하여 복합재료를 만들었을 때 다른 에폭시 수지를
사용한 경우에 비하여 높은 Tg를 나타낸 것을 확인할 수 있어 이를 경화제로 선정하였다[10]. 그리고 이방성으로 인한 물성 차이를 보완하기 위해
충전제로 Tin(IV) oxide를 사용하였다. Tin(IV) oxide는 가시광선 영역에서 투명하며 화학적으로 안정하다는 장점을 가지고 있다. 또한
31.38 W/m*K의 높은 열전도도를 가져 복합재료의 열적 특성 향상에 도움을 줄 것으로 예상된다[11]. 본
연구에서는 BP_SAA_Tin(IV) oxide
system의 열안정성을 파악하기 위해 열중량 분석기(TGA)를 사용하여 초기 열분해 활성화에너지를 Flynn-wall, Kissinger
method를 사용해 계산하여 확인하였으며, 열전도도 측정기(LFA)를 사용하여 열전도도를 측정하였다[12,13].
2.1 시료 및 시약
4,4’-dihydroxybiphenyl(97%), Benzyl trimethyl ammonium bromide(99%), Tin(IV) oxide(100 nm)는
Sigma-Aldrich사에서, Epichlorohydrin(99%), methyl alcohol(99.8%),
sulfanilamide(98%), sodium hydroxide(98%)는 삼전화학에서 구입하였다. 모든 시약은 정제 없이 사용하였다.
2.2 Diglycidyl
ether of 4,4’- Bisphenol(DGEBP)의 합성
4,4’-dihydroxybiphenyl 10 g, benzyl
trimethyl ammonium bromide 0.371 g,
epichlorohydrin 85 ml를 4구 플라스크에 넣고 온도는 120oC로 유지하며
reflux를 실시하여 질소 기류 하에서 마그네틱 바를 이용해서 300 rpm으로 교반한다. 1시간 교반 후 15 w/v% NaOH용액 50 ml를 dropping
funnel을 이용하여 약 3시간에 걸쳐서 첨가한다. 상온에서 얻어진 백색의 덩어리에 남아 있는 epichlorohydrin과 NaOH용액을 제거하기
위해 증류수와 메탄올을 이용하여 각각 2번씩 수세하고, 60oC에서 8시간 이상 진공건조를 하여 DGEBP를 얻는다[10].
2.3 에폭시 경화
경화제로는 sulfanilamide를 사용하였다. Sulfanilamide는 반응이 가능한 수소가 양 말단에 4개 존재하고 BP는 말단에 에폭시기가 2개가 있으므로
당량비를 1:2로 조절하였다. 용매는 에탄올을 사용하였고 Tin(IV) oxide는 3, 5, 7 wt% 비율로 비이커에
넣고 마그네틱 바를 이용하여 12시간 분산시킨 후 초음파 처리 하였다. 분산 후 테플론 디쉬에 옮겨 담고 150oC 11시간 동안 경화하였다.
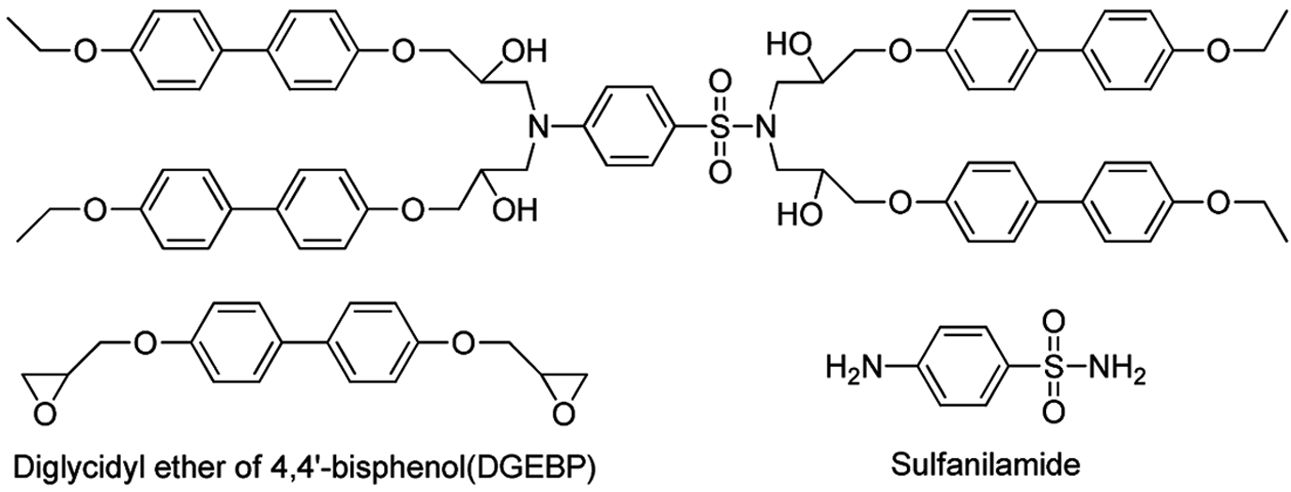
Fig. 1에 BP, SAA 및 이들의 경화 구조를 보였다.
2.4 특성 분석
Scanning Electron Microscope(SEM): 단면을 백금으로 코팅한
후 Carl Zeiss사의 SEM(SIGMA)을 이용하여 이미지를 얻었다. Tin(IV) oxide 3-7 wt%를 각각 분산시켜
경화 한 에폭시의 파단면을 촬영하였다.
Energy Dispersive Spectormeter (EDS): Matrix내의 Tin(IV) oxide의 분산성을 확인하기 위해 EDS분석을 수행하였다. SEM과 마찬가지로 Zeiss사의
SIGMA를 사용하였으며 WD는 8.5 mm, 가속전압은 20 kv로 설정하여 이미지를
얻었다.
Differential Scanning Calorimetry(DSC): Perkin-Elmer사의
DSC를 이용하여 질소 기류 하에서 10oC/min의 속도로 20-200oC까지 측정하였다.
Cross-polarization Microscope(POM): Nikon사의 OPTIPHOT-POL을 사용하였고,
heat-stage를 이용하여 분당 1oC/min의 속도로 승온, 냉각하여 액정 사진을 얻었다.
Thermogravimetric Analysis (TGA): METTLER TOLEDO 사의 DSC/TGA1을 사용하여
질소기류 하에서 25-1000oC까지 측정하였다. 각 샘플 당 5, 10, 20, 40oC/min의 승온 속도로
측정하여 이전 논문에서와 동일한 방법으로 활성화 에너지를 계산하였다[14].
Laser Flash Apparatus (LFA): NETZCH사의
LF457을 사용하여 열전도도를 측정하였다. 질소 기류 하에서 DSC를 사용하여 -10oC에서 40oC의 온도 범위내에서 열용량을
측정하였고, 상온에서의 열확산도를 측정해 열전도도를 구하였다.
|
Fig. 1 Schemetic image of crosslinked junction with BP and SAA |
3.1 합성된 에폭시의 액정성 확인
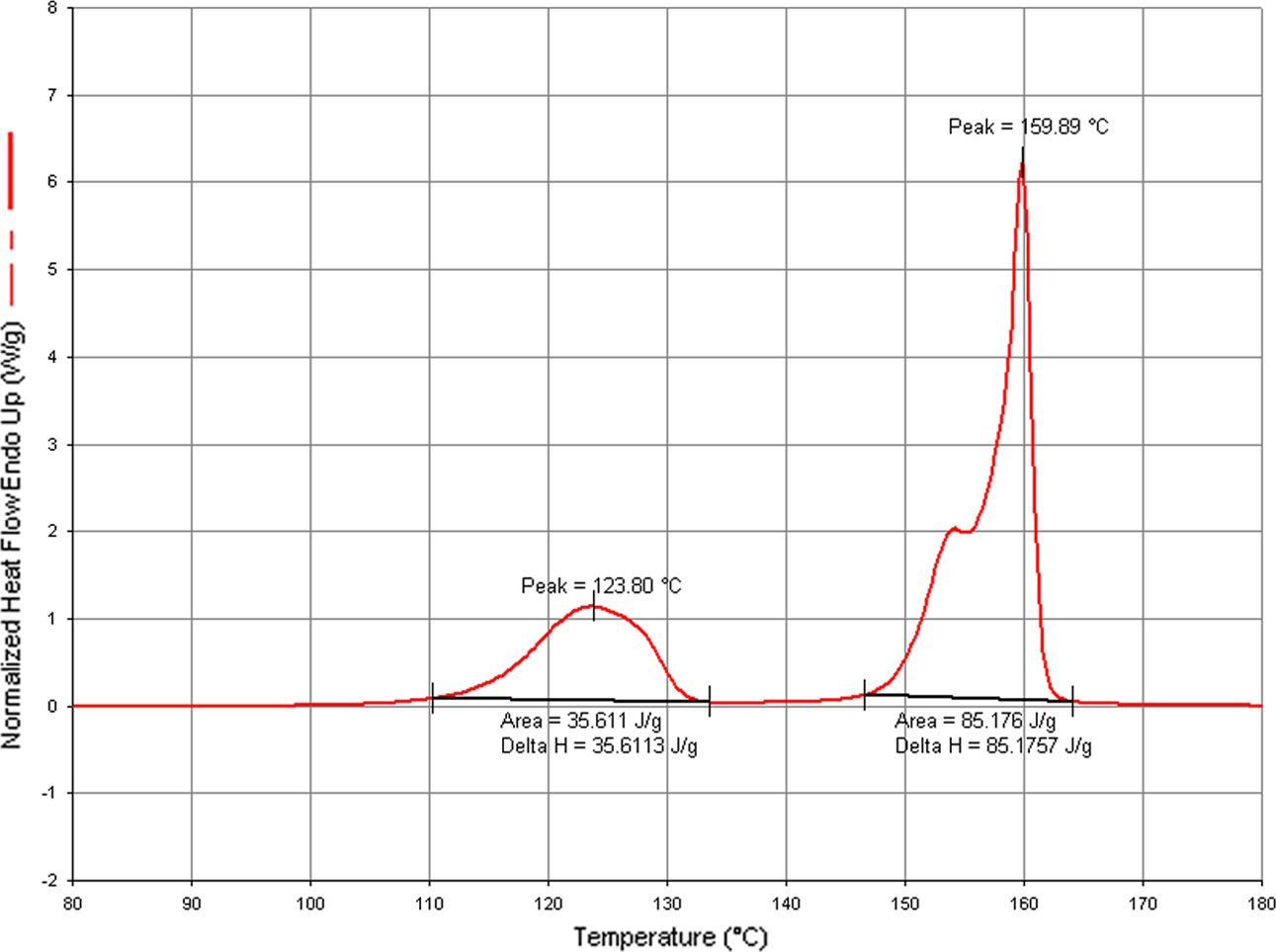
이전 논문에서와 같이 DSC와 POM을 사용하여 125oC에서 159oC 사이에서 액정성을 나타내는
것을 확인하였다[14]. 이를 Fig. 2, 3에 나타내었다.
3.2 Filler의 분산성 확인
EDS와 SEM을 이용하여 경화된 에폭시 복합재에서의 Tin(IV) oxide의 분산성을 확인하였는데, Fig. 4에서 보이는 바와 같이
시료전반에 Tin(IV) oxide가 분산된 것을 확인할 수 있다.
3.3 TGA를 이용한 열분해 활성화
에너지 측정
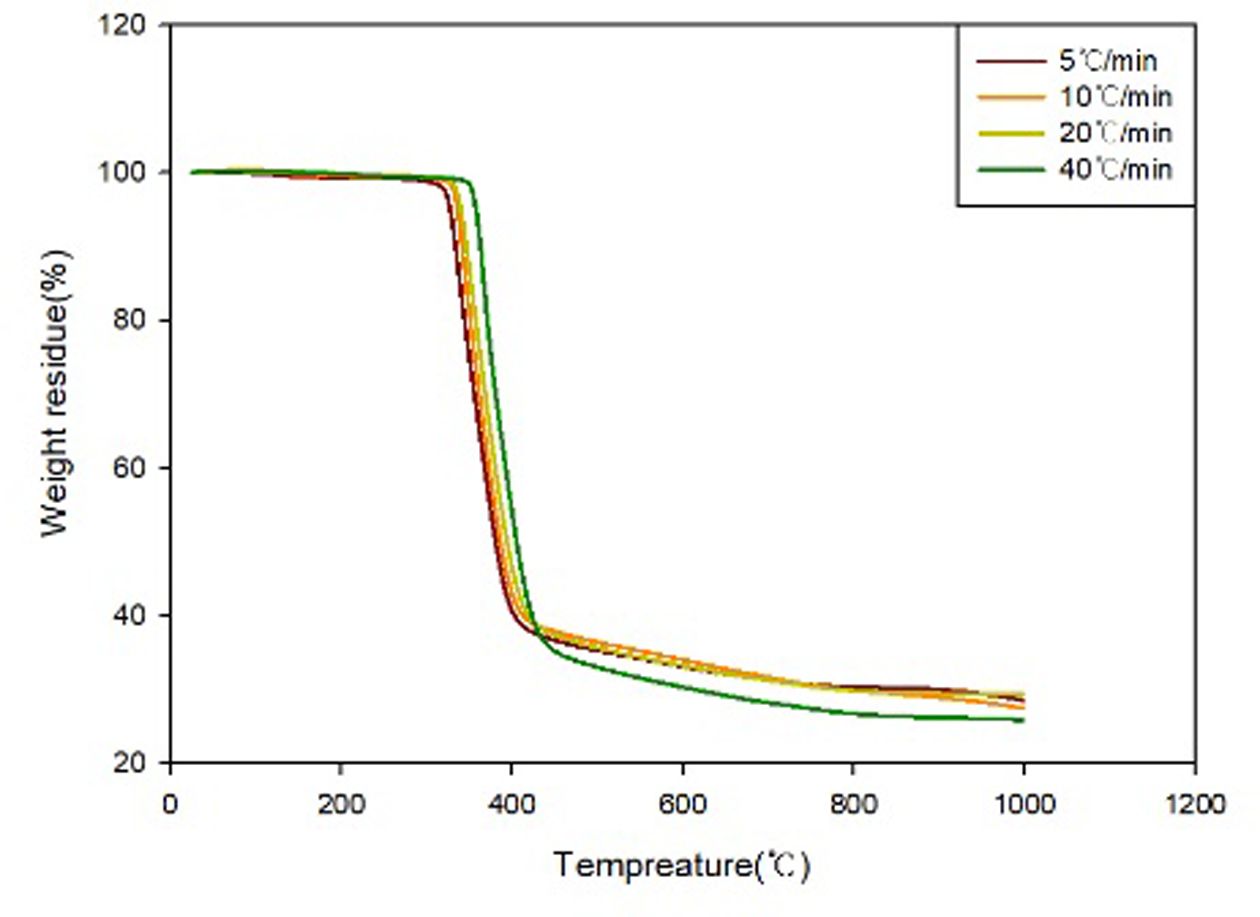
TGA측정은 5, 10, 20, 40oC의 승온 속도로 25oC에서 1000oC까지 범위를 설정하여 각
샘플 별로 측정을 하였다. BP-SAA-Tin oxide 5 wt% system의 비등온
열분해 그래프를 Fig. 5에 나타내었다.
활성화 에너지를 구하기 위해 위의 그래프를 Kissinger method와 Flynn-wall method를 사용하여 분석하였다[15].
Kissinger method는 최대 분해 속도일 때의 값인 식 (1)을 적용하여 식 (2)와 같이 나타내었다[16].
여기서 우항은 최대 분해 속도의 값이고, TP는 이때의 온도를 나타내며 Eα를 기울기로 나타낸다.
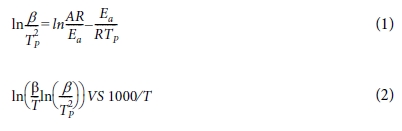
Flynn-wall method는 해당하는 분해 %의 온도에 대한 값을 적용하는 방법이며 식 (3)과 같이 계산하여 식 (4)로 나타내었다[17]. Kissinger
method와 유사하게 우항은 물질의 분해 %에 대한 온도이며, TP는 이때의 온도를 나타내며 Eα를 기울기로
나타낸다.
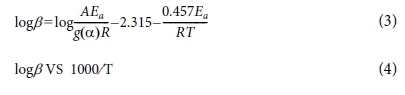
두 방법은 Arrhenius 식을 기반으로 비등온 열분해 거동을 구하는 방법이므로 근사치를 취하게 되어 오차가 발생할 가능성이 존재하므로 두 종류의 방법을 모두 계산하여 경향성을 확인하였다.
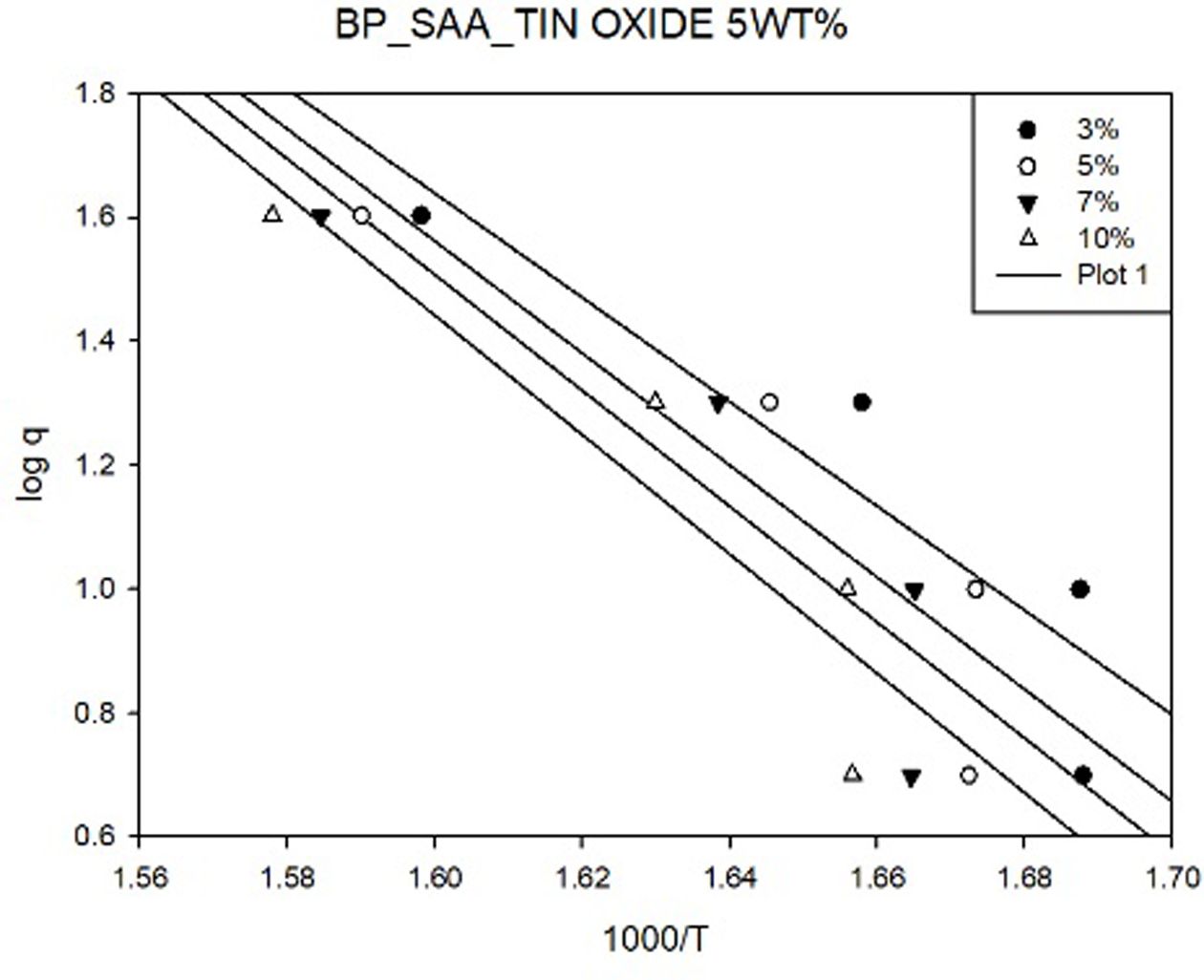
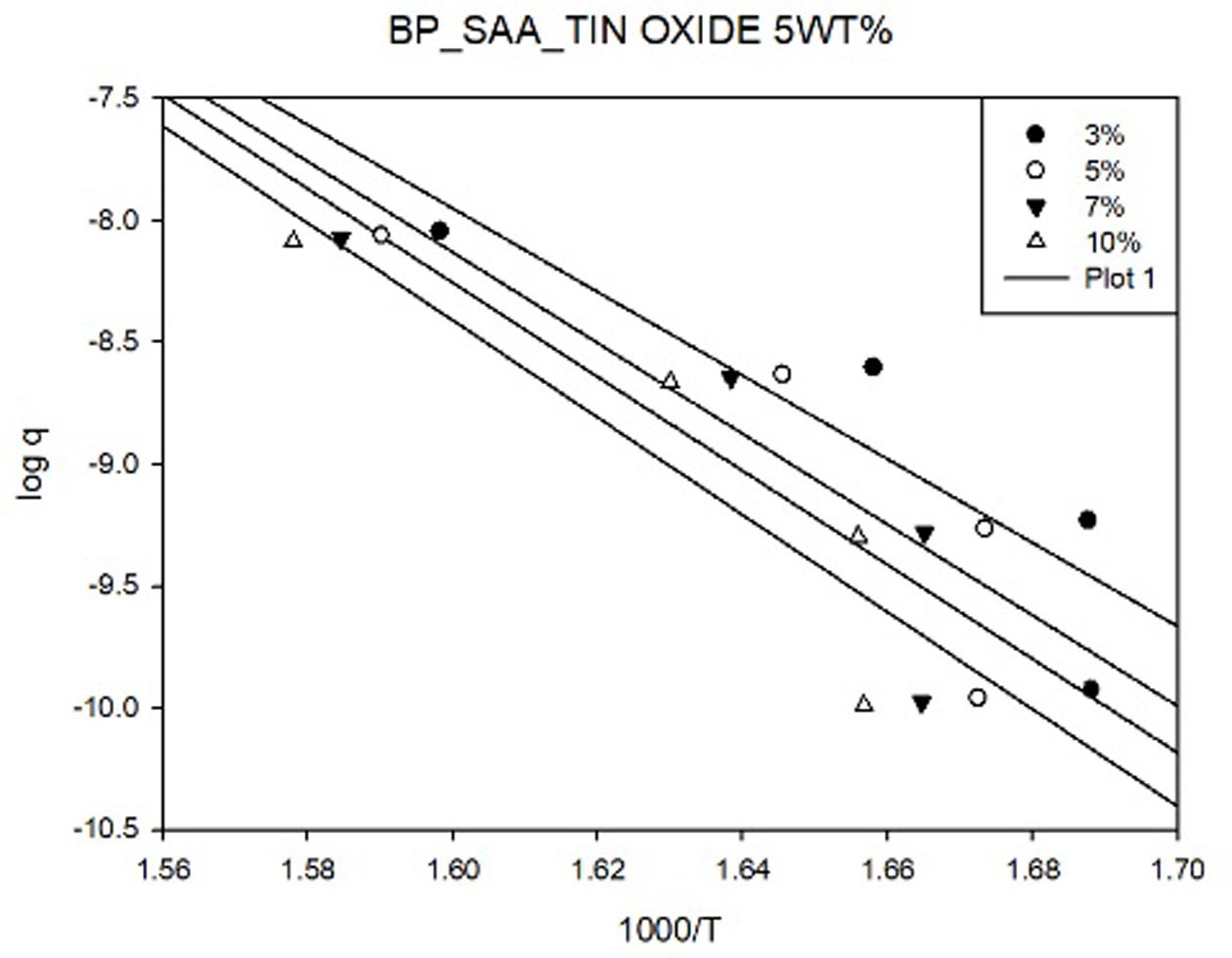
Fig. 6에 Flynn-wall 방법에 의해 구한 그래프를, Fig. 7에
Kissinger 방법에 의해 구한 그래프를 나타내었다. 또한 각각의 플롯에서 기울기를 이용해 활성화 에너지를 계산하였고, 이를 Fig. 8과 9에 나타내었다.
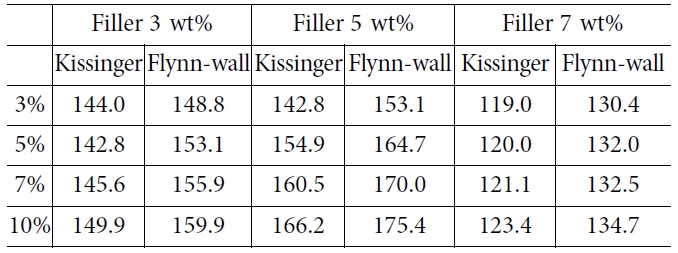
이를 이용해 무게비에 따른 활성화 에너지 변화를 Table 1에 나타내었다.
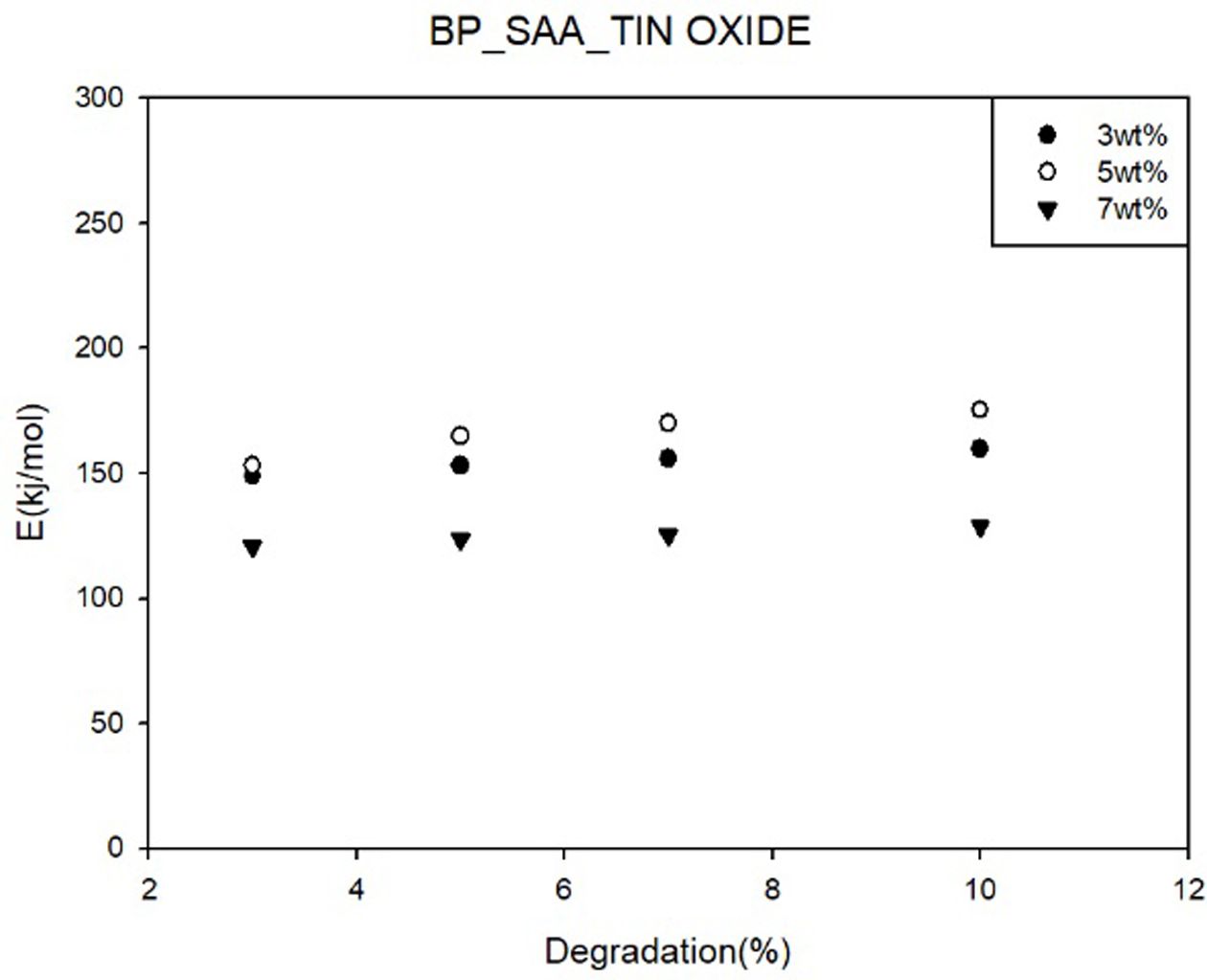
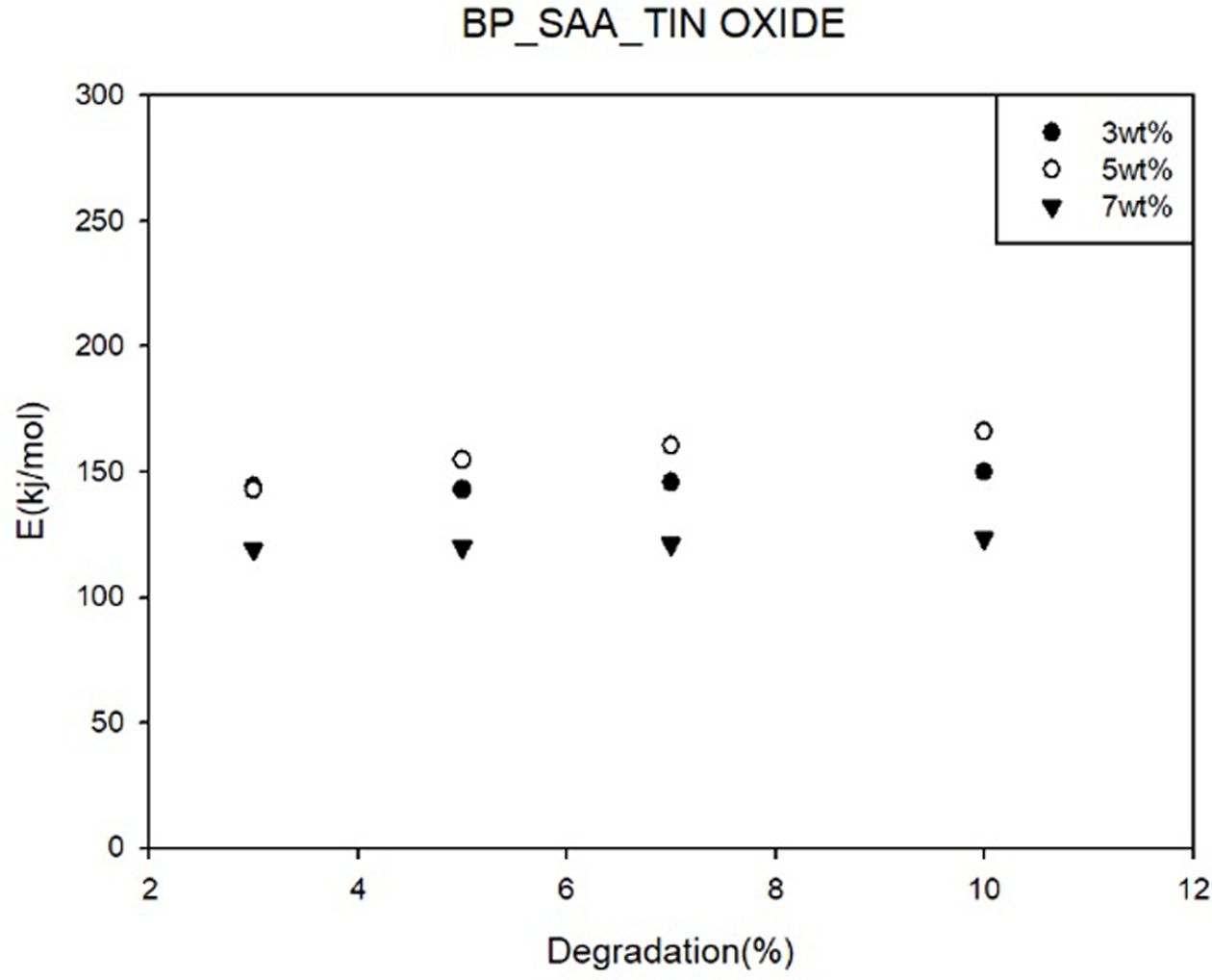
Tin(IV) oxide의 함량의 증가에 따라 3 wt%에서 5 wt%까지는 분해에 필요한
활성화 에너지가 증가하였지만 7 wt%의 경우 분해에 필요한 활성화 에너지가 오히려 감소하는 것을 확인할 수 있었다. 이는 함량
증가에 따른 filler의 응집에 의해 액정 형성시 방해요인으로 작용하여 활성화 에너지가 감소하는 것으로 파악된다
3.4 LFA를 이용한 열전도도
측정
LFA를 이용한 열전도도 측정 결과는 Fig. 10에 나타내었다.
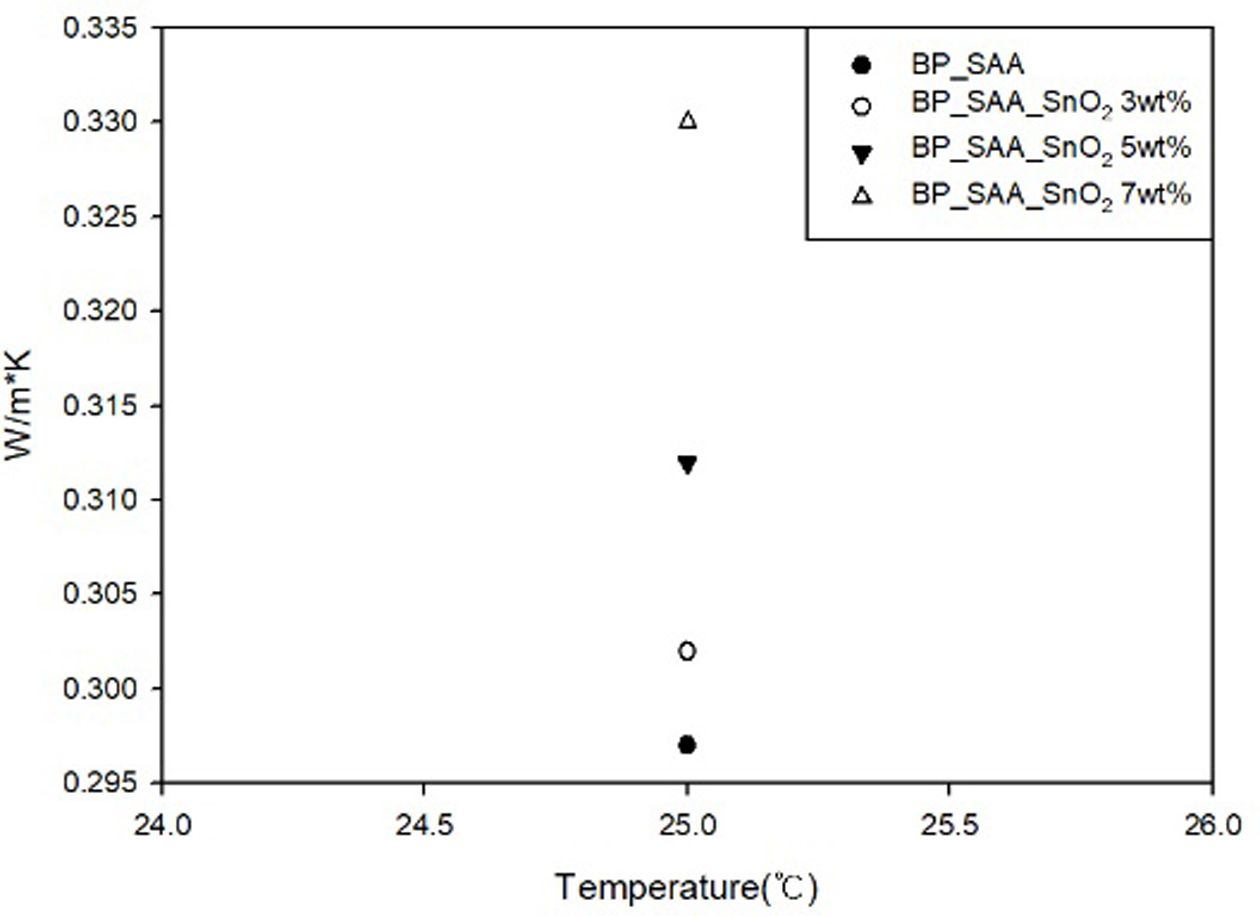
Filler 함량의 증가에 따라 열전도도가 증가하는 양상을 볼 수 있는데, 이는 filler가 열을 전달하는 경로를 형성해 열을 전달하는 것으로
추측된다.
|
Fig. 2 DSC thermogram of BP |
|
Fig. 3 POM image of BP; 150oC |

|
Fig. 4 SEM and EDS Image of BP-SAA-Tin(IV) oxide System: Tin(IV) oxide 5 wt% |
|
Fig. 5 TGA graph of BP-SAA-Tin(IV) oxide 5 wt% system |
|
Fig. 6 Flynn-wall plots of BP-SAA-Tin(IV) oxide 5 wt% |
|
Fig. 7 Kissinger plots of BP-SAA-Tin(IV) oxide 5 wt% |
|
Fig. 8 Activation energy of Flynn-wall method; BP-SAA-Tin(IV) oxide |
|
Fig. 9 Activation energy of Kissinger method; BP-SAA-Tin(IV) oxide |
|
Fig. 10 Heat capacity of BP-SAA-Tin(IV) oxide |
액정 에폭시 BP를 합성하고 전기적으로 우수한 물성을 갖는 Tin(IV) oxide를 충전제로 선택하여 분산 및 경화시킨 후 열분해시 필요한 활성화 에너지를 측정하고, LFA를 이용해 열전도도를 측정하였다.
그 결과 Filler 함량 증가에 대해 초기 열분해 활성화 에너지는 5 wt%에서 최고치를 나타낸
반면 열전도도는 함량이 증가할 수록 증가하는 것을 확인하였다. 이는 함량 증가에 따라 filler가 열전달 경로를 더 많이 형성해 열전도도가 증가하는
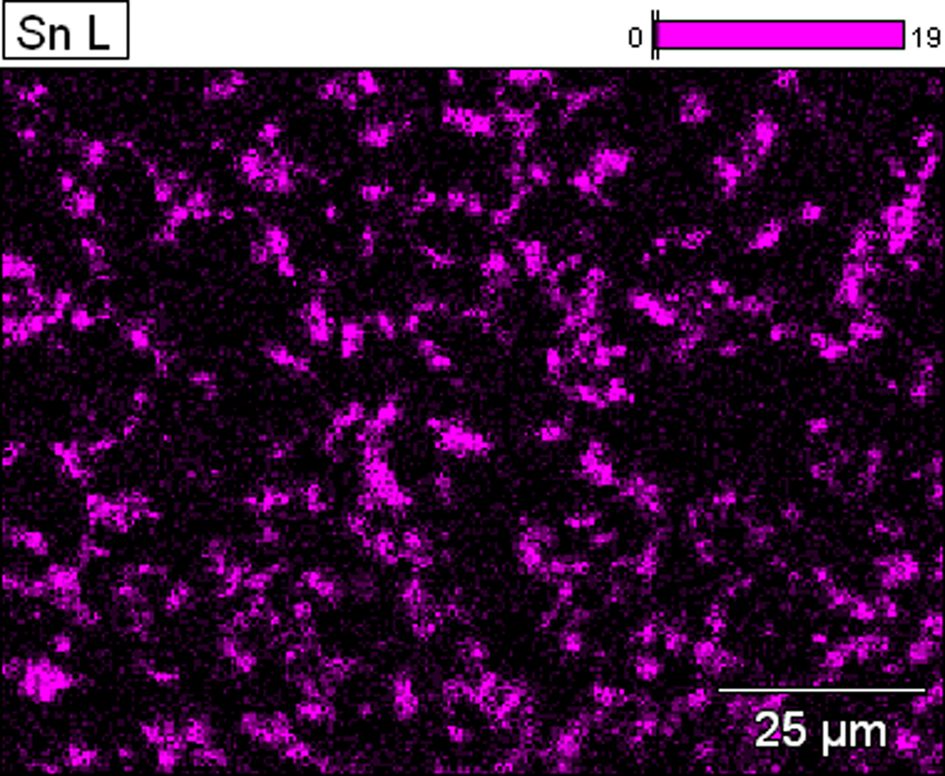
것으로 파악이 되며, 반면에 열분해 활성화 에너지의 경우. Fig. 11의 EDS 이미지에서
확인할 수 있었듯 응집에 의한 감소가 발생한 것으로 추정된다. 따라서 복합재료의 열전도도와 내열성을 동시에 증가시키기 위해서는 filler의 표면개질이나
가공을 처리를 진행해 분산성을 높이면 함량에 따라 열분해 활성화 에너지 또한 증가할 것으로 추정된다.
|
Fig. 11 SEM Image of BP_SAA_Tin(IV) oxide system |
본 연구는 한국연구재단의 기초과학연구 프로그램 지원으로 수행되었습니다(NRF-2018R1A2B60004512).
- 1. Lu, M.G., Shim, M.J., and Kim, S.W., “Thermal Degradation of LC Epoxy Thermosets,” Journal of Applied Polymer Science, Vol. 75, No. 12, 2000, pp. 1514-1521.
-

- 2. Li, Y., Badrinarayanan, P., and Kessler, M.R., “Liquid Crystalline Resin Based on Biphenyl Mesogen: Thermal Characterization,” Polymer, Vol. 54, No. 12, 2013, pp. 3017-3025.
-

- 3. Park, J.J., “Mechanical Properties of Epoxy Alumina Multi-composites,” Journal of the Korean Institute of Electrical and Electronic Material Engineers, Vol. 29, No. 12, 2016, pp. 796-802.
-

- 4. Liu, J., Wang, C., Campbell, G.A., Earls, J.D., and Priester, R.D., “Effects of Liquid Crystalline Structure Formation on the Curing Kinetics of an Epoxy Resin,” Journal of Polymer Science Part A: Polymer Chemisrty, Vol. 35, No. 6, 1997, pp. 1105-1124.
-

- 5. Yeo, H., Islam, A.M., You, N.H., Ahn, S.H., Goh, M.J., Hahn, J.R., and Jang, S.G., “Characteristic Correlation between Liquid Crystalline Epoxy and Alumina Filler on Thermal Conducting Properties”, Composites Science and Technology, Vol. 141, 2017, pp. 99-105.
-

- 6. Schultz, W.J., and Chartoff, R.P., “Photopolymerization of Nematic Liquid Crystal Monomers for Structure Applications: Molecular order and Orientation Dynamics,” Polymer, Vol. 39, No. 2, 1998, pp. 319-325.
-

- 7. Kim, Y.S., Jung J., Yeo, H.U., You, N.H., Jang, S.G., Ahn, S.H., Lee, S.H., and Goh, M.J., “Development of Highly Thermal Con-ductive Liquid Crystalline Epoxy Resins for High Thermal Dissipation Composites,” Composites Research, Vol. 30, No. 1, 2017, pp. 1-6.
-

- 8. Hirn, B., Carfagna, C., and Lanzetta, R., “Linear Precursors of Liquid Crystalline Thermosets,” Journal of Materials Chemistry, Vol. 6, No. 9, 1996, pp. 1473-1478.
-

- 9. Lee, J.Y., Shim, M.J., and Kim, S.W., “Synthesis of Liquid Crystalline Epoxy and Its Mechanical and Electrical Characteris-tics-Curing Reaction of LCE with Diamines by DSC Analysis,” Journal of Applied Polymer Science, Vol. 83, No. 11, 2002, pp. 2419-2425.
-

- 10. Su, W.-F.A., Chen, K.C., and Tseng, S.Y., “Effects of Chemical Structure Changes on Thermal, Mechanical, and Crystalline Proper-ties of Rigid Rod Epoxy Resins,” Journal of Applied Polymer Science, Vol. 78, No. 2, 2000, pp. 446-451.
-

- 11. Kang, S.S., Lee, S.H., Jang Y.S., and Park S.C., “The Electrical and Optical Characteristics of ATO Films Prepared by RF Magnetron Sputtering Method,” Journal of Korean Ophthalmic Optics Society, Vol. 15, No. 4, 2010, pp. 299-305.
- 12. Moon, H.J., Kim, K.H., Hwangbo, S.J., and Choi, S.H., “Thermal Decomposition Activation Energy of Liquid Crystalline Epoxy Composite with Zirconia Filler,” Journal of the Korean Fiber Society, Vol. 52, No. 3, 2015, pp. 206-214.
-

- 13. Choi, J.R., and Park, S.J., “A Study on Thermal Conductivity and Fracture Toughness of Alumina Nanofibers and Powders-filled Epoxy Matrix Composites,” Polymer Korea, Vol. 37, No. 1, 2013, pp. 47-51.
-

- 14. Moon, H.J., and Cho, S.H., “Thermal Decomposition Behavior of LCT Composites Using Boron Nitride Filler,” Textile Science and Engineering, Vol. 53, No. 4, 2018, pp. 293-298.
-

- 15. Venkatesh, M., Ravi, P., and Tewari, S.P., “Isoconversional Kinetic Analysis of Decomposition of Nitroimidazoles: Friedman method vs Flynn-Wall-Ozawa Method,” The Journal of Physical Chemistry A, Vol. 117, No. 40, 2013, pp. 10162-10169.
-

- 16. Kissinger, H.E., “Reaction Kinetics in Differential Thermal Analysis,” Analytical Chemistry, Vol. 29, No. 11, 1957, pp. 1702-1706.
-

- 17. Flynn, J.H., and Wall, L.A., “General Treatment of the Thermogravimetry of Polymer,” Journal of Research of the National Bureau of Standards-A. Physics and Chemistry, Vol. 70A, No. 6, 1996, pp. 487-532.
-

 This Article
This Article
-
2020; 33(1): 25-29
Published on Feb 28, 2020
- 10.7234/composres.2020.33.1.025
- Received on Apr 26, 2019
- Revised on Feb 28, 2020
- Accepted on Feb 28, 2020
 Services
Services
Shared
 Correspondence to
Correspondence to
- Seung Hyun Cho
-
*† Department of Organic Materials and fiber Engineering, Soong-sil University
- E-mail: scho@ssu.ac.kr






 Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.
Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.